Qu’est-ce que la CEC et pourquoi est-ce important?


Nous recevons parfois des questions par rapport à la CEC ou à la capacité de rétention nutritionnelle de nos produits PRO-MIX. Les deux questions se rapportent à la CEC. Mais la CEC, c’est quoi?
CEC est l’acronyme de « capacité d’échange cationique », qui se réfère à la capacité d’échange et de rétention des nutriments minéraux d'un substrat de culture. Dans cet article, nous examinons ce qu’est la CEC et son importance.
Comprendre la capacité d’échange cationique (CEC)
Pour comprendre ce qu’est la CEC, nous devons revoir un peu de chimie. Un engrais conventionnel se présente sous forme de sels. Lorsque mélangés avec de l’eau, ces sels de dissocient, laissant des nutriments chargés individuellement. Par exemple, le nitrate de calcium (un sel) se sépare dans l’eau en calcium et en nitrate :
Ca(NO3)2 + eau = Ca++ + 2 NO3-
Le calcium et le nitrate ont tous les deux une charge électrique. Le calcium a une charge positive, ou cation, et le nitrate a une charge négative, ou anion.
La figure 1 démontre tous les éléments végétaux et leur charge. Pour les engrais organiques, la même règle s’applique ; les microbes séparent les molécules complexes en les mêmes éléments individuels que dans la figure 1.
| Cations (charge positive) | Anions (charge negative) |
|---|---|
| Ammonium (HN4*) | Bore (Borate - BO3*) |
| Calcium (Ca**) | Chloride (CI*) |
| Cuivre (Cu*) | Nitrate (NO3*) |
| Hydrogène (H*) | Phosphate (H2PO4*) |
| Fer (Fe**) | Sulfate (SO4**) |
| Magnésium (Mg**) | |
| Manganèse (Mn**) | |
| Potassium (K*) | |
| Sodium (Na*) | |
| Zinc (Zn**) |
La charge négative des sols et des substrats de culture
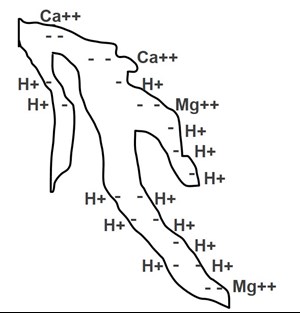
Les sols et les substrats de culture (tourbe, vermiculite, écorce, coir de coco, argile calcinée, etc.) ont des charges électriques à leur surface. S’il y a une charge négative à la surface d’une particule de substrat de culture, elle contribue à la capacité d’échange cationique.
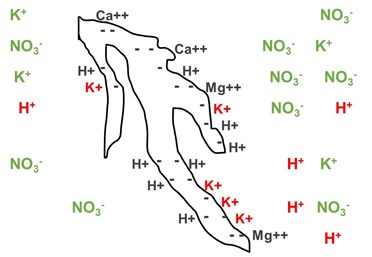
Les éléments chargés positivement (cations) se lient à ces sites négatifs sur les particules de substrat, et peuvent par la suite être échangés pour un autre élément utilisé par la plante. Plus il y a de sites chargés négativement sur ces particules, plus la capacité d’échange cationique du substrat est grande.
La charge positive des sols et des substrats de culture
Les sols et les substrats de cultures peuvent aussi avoir des charges positives qui attirent des particules à charges négatives. Ces sites positifs contribuent à la capacité d’échange d’anions du substrat de culture. En comparaison, la capacité d’échange cationique est plus importante dans un substrat de culture que la capacité d’échange anionique.
Les éléments, du plus fort au plus faible (CEC)
La force de liaison des éléments à ces sites d’échanges varie du type d’élément et sa charge (+1, +2, etc.) L’image ci-dessous montre quels éléments sont les mieux retenus et lesquels sont les moins retenus.
Mieux retenus ----------------> Moins retenus
H+ > Ca++ > Mg++ > K+ = NH4+ > Na+
Cela signifie que le calcium (Ca++) et le magnésium (Mg++) sont moins prônes à de détacher du site d’échange que le sodium (Na+), le potassium (K+) ou l’ammonium (NH4+). Par conséquent, puisque le potassium est un cation faiblement absorbé et qu’il est moins susceptible de se lier à un site d’échange si le calcium est présent, le potassium est plus susceptible d’être lessivé du substrat
Les avantages d’une CEC élevée en horticulture
Les avantages d’une CEC élevée sont non seulement que le sol ou le substrat de culture peut emmagasiner beaucoup d’éléments d’engrais et les restituer aux plantes plus tard, mais aussi la CEC peut aider la plante à résister à un changement de pH. Par exemple, en ajoutant de la chaux à un sol argileux acide, le calcium et le magnésium peuvent déplacer l’hydrogène (ions acides) des sites CEC.
L’hydrogène se lie au carbonate issu de la chaux, provoquant une augmentation du pH du sol argileux. Plus le sol retient les ions d’hydrogène, plus il faudra de la chaux pour ajuster le pH du sol.
Quand un engrais est appliqué sur un sol, de nombreux éléments de l’engrais pourraient se lier aux sites CEC. Conséquemment, un sol avec une CEC élevée nécessitera une application plus fréquente d’engrais pour compenser. Si les niveaux de fertilité diminuent dans le sol, certains de ces éléments fertilisants peuvent être échangés et devenir disponible pour l’utilisation des plantes.
Bien que la CEC ait une certaine valeur dans les substrats de culture, elle n’est pas aussi importante en ce qui concerne l’échange de nutriments et gestion du pH qu’elle ne l’est avec le sol.
La valeur CEC exprimée en poids vs en volume
La capacité d’échange cationique est mesurée en milliéquivalent pour 100 grammes de substrat de culture (meq/100g). Cependant, elle pourrait également être mesurée en meq/100cm³.
Typiquement, la valeur CEC dans le sol ou dans divers éléments de substrat est listée comme dans la Figure 1 ci-dessous.
| Composantes / Mélange | CEC (meq / 100g) |
|---|---|
| Argile fine | 56-63 |
| Argile grossière | 22-52 |
| Limon | 3-7 |
| Tourbe de sphaigne | 100-120 |
| Houmous de tourbe | 200 |
| Vermiculite | 150 |
| Perlite | 1.5 |
| Écorces vieillies | 40-60 |
| 50% Tourbe, 50% Vermiculite | 141 |
En regardant la figure 1, il est clair que la CEC de la tourbe et de la vermiculite est plus élevée que celle de l’argile. Cette affirmation est vraie sur une base pondérale, puisque la CEC est exprimée par meq / 100 grammes. Cependant, les contenants sont remplis en fonction de leur volume et non pas le poids qu’ils contiennent. Il est donc plus précis d’exprimer la CEC en volume, puisque des plantes qui poussent dans un contenant n’ont accès qu’aux nutriments du substrat présent dans le contenant.
Les valeurs changent en fonction du volume
Ainsi, quand une CEC est exprimée en volume, les valeurs numérales changent, tel qu’indiqué dans le tableau 1 ci-dessous.
| Mesure | Terre de champ | 1 Tourbe: 1 Vermiculite |
|---|---|---|
| CEC (meq/100 g) | 20 | 141 |
| Densité apparente (g/cm3) | 1.3 g/cm3 | 0.1 g /cm3 |
| Volume du contenant (cm3/pot) | 1250 cm3 | 1250 cm3 |
| CEC (meq/pot) | 325 | 176 |
Exprimée en poids dans la première ligne du tableau 1, la CEC de 20 meq/100g de la terre de champ est bien moins élevée que la CEC de 141 meq/100g du substrat composé de tourbe/vermiculite. La deuxième ligne du tableau démontre que la masse volumique de la terre de champ est 13 fois plus lourde que le mélange de tourbe et de vermiculite.
Si ces deux substrats étaient ajoutés dans des pots individuels de volume égal (1250 cm³), la CEC de la terre de champ serait de 325 meq/pot, soit presque deux fois plus élevée que la CEC de 176 meq/pot du substrat de tourbe/vermiculite.
La CEC masquée par d’autres variables
Des recherches par John Biernbaum et Bill Argo ont démontré que même si la CEC d’un substrat de culture a un effet sur la rétention des nutriments et sur la protection contre les légers changements de pH, d’autres variables exerçaient une influence plus importante sur le pH et la capacité nutritionnelle du substrat de culture.
L’apport en chaux dans un substrat de culture
Premièrement, le pH d’un substrat de culture est influencé de façon significative par son apport en chaux, l’acidité/la basicité potentielle de l’engrais utilisé, et l’alcalinité (teneur en carbonate et en bicarbonate) de l’eau. À long terme, tout changement dans ces variables a plus d’influence que la CEC sur le pH du substrat.
La rétention du calcium et du magnésium
Deuxièmement, les chercheurs ont découvert que le taux de rétention de calcium et de magnésium par les sites CEC peut être considéré comme important dans un substrat de culture avec une CEC élevée, mais pas en comparaison avec les quantités de calcium et de magnésium qui devront être ajoutées comme engrais pour éviter des carences nutritionnelles.
En d’autres mots, contrairement aux sols argileux qui peuvent contenir suffisamment de magnésium et de calcium dans leurs sites d’échanges pour nourrir les cultures pendant tout un cycle de croissance, les substrats de cultures ne peuvent tout simplement pas retenir tous ces nutriments. Des applications supplémentaires d’engrais sont donc nécessaires au cours du cycle de croissance. Résultat? Les producteurs ne dépendent pas de l’aide de la CEC pour nourrir les plantes cultivées dans un substrat de culture.
Le pH de la tourbe de sphaigne
Troisièmement, le pH du substrat de culture influence la CEC. Par exemple, si le pH de la tourbe de sphaigne augmente de 3.5 à 8, la CEC augmente aussi de 140 meq/l. À mesure que le pH de la tourbe de sphaigne s’élève, les ions d’hydrogène plus difficiles à déplacer se détachent des sites d’échange de cations, permettant à d’autres éléments, comme le calcium et le magnésium, de les remplacer.
Cependant, combien de cultures peuvent être cultivées à un pH de 8.0? En règle générale, les cultures se portent mieux lorsque le pH se situe entre 5.5 et 6.2, alors la CEC peut être moins élevée que selon les sources publiées.
Apprenez-en plus sur comment le pH d’un substrat de culture influence la disponibilité des nutriments.
Fournir des nutriments par la fertilisation
Même si un substrat de culture peut avoir une CEC convenable, celle-ci ne contribue que très peu à la rétention des nutriments ou la prévention d’un changement de pH, contrairement aux sols argileux. Si des nutriments sont nécessaires, les producteurs doivent les ajouter avec des engrais et non dépendre des sites d’échange de cation.
Ainsi, le pH d’un substrat de culture peut être manipulé facilement avec l’ajout de chaux, l’application d’engrais et/ou l’alcalinité de l’eau.
Lectures complémentaires et références :
- Argo, W.R. and J.A. Biernbaum. 1997. "The effect of root media on root-zone pH, calcium, and magnesium management in containers with impatiens." J. Amer. Soc. Hort. Sci. 122(2):275-284. https://www.researchgate.net/publication/279467327_The_Effect_of_Root_Media_on_Root-zone_pH_Calcium_and_Magnesium_Management_in_Containers_with_Impatiens
- Table 1. Biernbaum, J.A. 1992. "Root-Zone Management of Greenhouse Container-Grown Crops to Control Water and Fertilizer." Hort Technology 2(1):127-132. https://scholar.google.ca/scholar?q=Root-Zone+Management+of+Greenhouse+Container-Grown+Crops+to+Control+Water+and+Fertilizer.&hl=fr&as_sdt=0&as_vis=1&oi=scholart
- Figure 1. Source: Bunt, A.C. 1988. "Media and Mixes for Container Grown Plants." Second edition. Unwin Hyman Ltd., London https://home.czu.cz/storage/737/65060_A.-C.-Bunt-auth.-Media-and-Mixes-for-Container-Grown-Plants-A-manual-on-the-preparation-and-use-of-growing-media-for-pot-plants-Springer-Netherlands-1988-.pdf